Image by tawanlubfah de Getty Images Pro de Canva
La regulación de los medicamentos desempeña un papel crucial en el rápido crecimiento del sector farmacéutico tailandés, que se sitúa como el segundo mayor mercado farmacéutico y de salud de los consumidores del Sudeste Asiático, con unas ventas farmacéuticas que se prevé que alcancen los 14.1 billones de USD en 2040 a una tasa de crecimiento anual compuesto (TCAC) del 8,31%.
El sistema sanitario del país está supervisado por la Administración Tailandesa de Alimentos y Medicamentos (FDA), principal autoridad reguladora responsable de la aprobación, clasificación y supervisión de fármacos y productos sanitarios. Colabora con organismos internacionales como la OMS y la ASEAN para mantener las normas mundiales.
El proceso de solicitud de aprobación de medicamentos OTC y Rx se divide en dos partes principales:
- Autorización de instalaciones farmacéuticas, Registro y aprobación de productos farmacéuticos.
- Registro y aprobación de productos farmacéuticos.
La autorización de instalaciones farmacéuticas para productos farmacéuticos producidos en instalaciones en el extranjero requiere la autorización GMP de la FDA tailandesa. Tras obtener la licencia para una instalación farmacéutica o la autorización GMP, el siguiente paso es registrar el producto en la FDA. La documentación debe prepararse de acuerdo con el Expediente Técnico Común de la ASEAN (ACTD) y el Documento Técnico Común de la ICH (ICH CTD). El proceso de registro del medicamento puede durar hasta 155 días, pero el periodo de aprobación puede ampliarse, dependiendo del tipo de producto que se registre. La figura 1 ilustra un ejemplo del proceso de registro de medicamentos genéricos OTC y Rx.
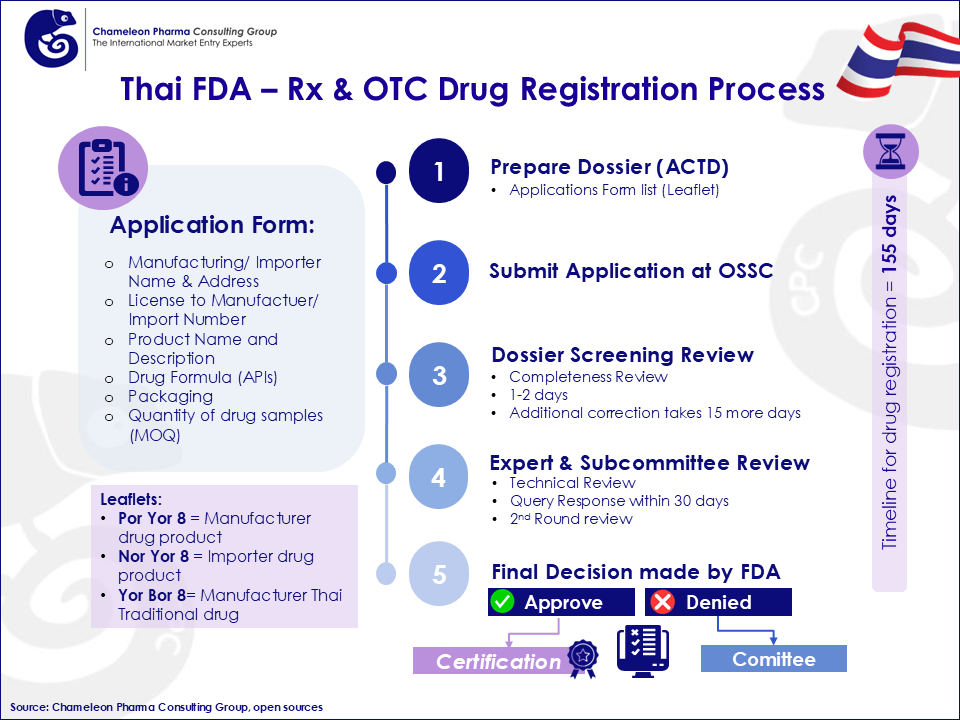
Figura 1: Proceso de registro de medicamentos de venta con y sin receta en Tailandia
El marco nacional tailandés sobre medicamentos: Aprobación de medicamentos OTC, farmacovigilancia y cobertura sanitaria
En cuanto a la aprobación nacional de medicamentos, el proceso implica rigurosos ensayos preclínicos y clínicos, junto con el registro y la vigilancia postcomercialización de la FDA tailandesa. La farmacovigilancia y el Centro Nacional se crearon en 1983, año en que Tailandia se adhirió al programa de la OMS para la Vigilancia Internacional de Medicamentos (WHOPIDM). La farmacovigilancia garantiza el seguimiento continuo de la seguridad de los medicamentos tras su aprobación, centrándose en los efectos adversos.
El marco de selección y reembolso de medicamentos se divide en tres niveles. Se gestiona principalmente a través de la Lista Nacional de Medicamentos Esenciales (NLEM), que consiste en la lista de reembolso farmacéutico para los tres regímenes de salud pública, a saber:
- El Régimen de Prestaciones Médicas de los Funcionarios (CSMBS)
- El Régimen de Seguridad Social (SSS)
- El Régimen de Cobertura Universal (RCU)
La UCS, también conocida como la «Tarjeta Dorada», la UCS tailandesa ha mejorado el acceso a la asistencia sanitaria y contribuido al crecimiento económico tailandés durante los últimos 22 años. Más del 99% de los ciudadanos tailandeses están cubiertos por la asistencia sanitaria financiada por los impuestos, que incluye ayudas para enfermedades raras y tratamientos de alto coste, aunque el acceso a los medicamentos en las zonas rurales sigue siendo un reto.
En esencia, Tailandia ofrece una atractiva oportunidad de inversión en el sector farmacéutico, respaldada por un sólido marco normativo gestionado por la FDA tailandesa. El país garantiza un alto nivel de seguridad de los medicamentos mediante rigurosos procesos de aprobación y una farmacovigilancia activa, al tiempo que integra las mejores prácticas internacionales y las innovaciones digitales en materia de salud. Tailandia demuestra un firme compromiso con el acceso y la calidad de la atención sanitaria.
A pesar de los continuos retos, como la falsificación de medicamentos y el acceso rural, el enfoque proactivo del gobierno hacia la reforma reguladora y la innovación crea un mercado dinámico y prometedor para los inversores extranjeros. El cumplimiento normativo y legal se gestiona mejor a través de asociaciones con empresas locales. Por lo tanto, CPC aconseja a los promotores de negocios internacionales que den prioridad a la identificación de socios locales adecuados como un enfoque estratégico crucial.
Chameleon Pharma Consulting Group está especializado en proyectos de internacionalización, entrada en el mercado y regulación en las áreas de salud del consumidor, farmacia, complementos alimenticios, productos sanitarios y cosmética en América Latina, Europa, Asia, EE.UU./Canadá, Oriente Medio y ECE/CEI. Hemos completado más de 300 proyectos de entrada en mercados internacionales, ofreciendo:
- Análisis Sistemático de País y Producto (análisis de cartera),
- Identificación Sistemática de Socios Locales,
- Registro y Asuntos Regulatorios,
- Servicios de Transformación Digital (consultoría estratégica, e-learning, análisis de redes sociales, optimización SEO y otros).
Para sus preguntas individuales, póngase en contacto con nosotros por correo electrónico en service@chameleon-pharma.com.




